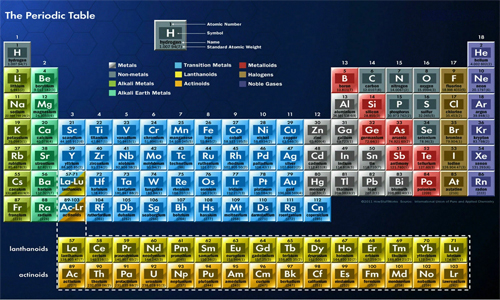
Strukur Atom : Nomor Atom dan Massa Atom
ittekcno.blogspot.com – pada artikel ini kita akan sama-sama membahas dan mempelajari tentang nomor atom dan massa atom
Pengenalan Atom
Atom merupakan partikel yang sangat kecil dengan massa yang secara proporsional kecil pula. Istilah atom berasal dari bahasa yunani yaitu “atomos” dimana a artinya “tidak” dan “tomas” artinya “dipecah atau dibagi”, sehinggan atom dapat diartikan sebagai suatu partikel atau komponen yang tidak dapat dibagi lagi.
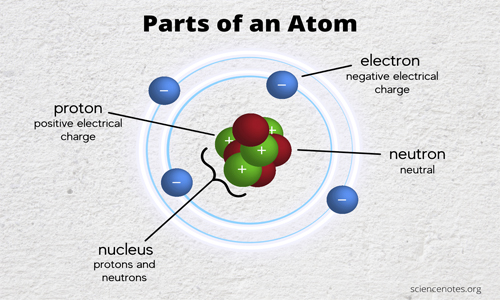
Atom terdiri dari inti atom yang bermuatan positif dan electron bermuatan negative yang bergerak mengelilingi inti atom. Inti atom terdiri atas proton yang bermuatan positif dan neutron yang bermuatan netral ( kecuali pada inti atom hydrogen yang tidak memilik neutron ), sedangkan electron-elektron yang mengelilingi inti atom terikat oleh gaya elektromagnetik.
Perhatikan gambar berikut :
Sekumpulan atom yang terdiri dari dua atau lebih atom yang saling berikatan melalui ikatan kimia disebut dengan molekul.
Konsep tentang atom yang merupakan komponen yang sangat kecil dan tidak dapat dibagi-bagi telah ada sejak ribuan tahun lalu, namun pemikiran tersebut masih versifat abstrak dan filosofis.
Istilah atom sendiri pertama kali dicetuskan oleh ilmuwan yunani yang bernama demekritosn pada abad ke-4 masehi.
Demokritos berpendapat bahwa atom merupakan benda padat yang tidak memiliki struktur internal serta terdapat ruang kosong untuk pergerakannya. Selain itu juga ia menjelaskan cara membedakan sifat atau material suatu atom dapat dilihat dari bentuk, massa, dan ukuran.
Namun, model demokritos ini tidak dibuktikan dengan eksperimen sehingga bernunculan teori-teori atom baru berdasarkan hasil riset.
Beberapa teori atom diantaranya sebagai berikut :
Teori Atom Dalton
Konsep atom yang sebelumnya dikemukakan oleh demokritos kemudian dikembangkan oleh john Dalton sesuai dengan namanya ini dikenal dengan teori atom Dalton. Adapun isi dari teori atom Dalton adalah sebagai berikut :
- Atom merupakan partikel terkecil dari suatu unsure yang tidak dapat dibagi-bagi.
- Atom-atom dengan unsure sejenis memiliki sifat sama, sedangkan atom dengan unsure berbeda nenukuju sifat yang berbeda.
- Reaksi kimia menghasilkan pemisahan ata penggabungan suatu atom
- Suatu atom dapat bersatu dengan lainnya menjadi sebuah molekul dengan perbandingan bulat dan sederhana.
Hipotesis Dalton digambarkan dengan model atom sebagai bola pejal seperti tolak peluru.
Sayangnya teiru Dalton tidak dapat menjelaskan bagaimana atom sebagai bola pejal dapat menghantaran arus listrik yang mana listrik adalah electron yang bergerak.
Denga kata lain Dalton tidak sempat membuktikan partikel lain yang menghantarkan arus listrik. Sebelum dipatahkan oleh ilmuwan setelahnya, teori atom Dalton dianut hingga ratusan tahun.
Teori Atom Thompson
Teori atom Thompson merupakan teori yang dikembangkan dari teori sebelumnya. Thompson menemukan adanya partikel yang memiliki muatan negative pada sebuah atom.
Partikel tersebut kemudian dikenal dengan nama electron. Thompson menggambarkan model atomnya seperti bola roti dengan taburan kismis yang mana bola itu padat bermuatan positif dan dipermukaanya tersebut electron bermuatan negative.
Sayangnya model atom Thompson tidak dapat menjelaskan susunan muatan positif dan negative dalam atom
Model Atom Rutherford
Teori atom ruutherford dicetuskan oleh ernest Rutherford yang merupakan ahli fisika kelahiran selandia baru. Beliau merupakan salah satu tokoh yang berjasa dalam pengembangan model atom.
Setelah melakukan eksperimen panjang, ia berhasil menemukan adanya inti atom yang berada di dalam atom itu sendiri, yang mana inti atom bermuatan positif sekaligus menjadi pusat dan inti atom tersebut dikelilingi oleh awan electron bermuatan negative.
Gambar atom Rutherford digambarkan sebagaimana planet mengelilingi matahari.
Namun model atom Rutherford tidak dapat menjelaskan mengapa electron tidak jatuh kedalam inti atom.
Model Atom Bohr
Pencetus dari teori atom ini adalah neils bohr yang merupakan ilmuwan asal Denmark. Teori ini dikembangkan setelah melakukan percobaan pada spectrum atom hydrogen. Inilah yang membuat bohr menemukan teori layaknya peredaran planet yang mengelilingi tata surya.
Adapun teori tentang sifat arom yang didapat dari pengamatan bohr yaiut ;
- Atom terdiri dari inti yang bermuatan positif dan dikelilingi oleh electron yang bermuatan negative di dalam suatu lintasan
- Electron bisa dipindahkan dari satu lintasan ke lintasan yang lain dengan menyerap atau memancarkan energi sehingga energi electron atom itu tidak akan berkurang
- Jika berpindah ke lintasan yang lebih tinggi, electron akan menyerap energi dan jika berpindah kelintasan yang lebih rendah, electron akan melepaskan energi.
- Kedudukan electron-elektron pada tingkat-tingkat energi tertentu disebut kulit-kulit electron
Hipotesis bohr adalah atom terdiri dari inti yang bermuatan positif dan dikelilingi oleh electron yang bermuatan negative di dalam suatu lintasan.
Model Atom Modern
Model atom modern merupakan bentuk pengembangan dari teori atom yang sudah ada sebelumnya yaitu teori atom bohr. Pada teori atom bohr dijelaskan bahwa electron mengelilingi atom dengan jarak tertentu yang disebut inti atom.
Namun, berbeda dengan teori atom modern yang menjelaskan inti atom tidak dapat dipastikan serta tidak diketahui letak posisinya. Terdapat 3 ilmuwan yang berperan dalam teori atom modern ini yaitu Louis victor de Broglie, Werner heinsberg, dan Erwin schrodinger.
Pada tahun 1923, Broglie mencetuskan sebuah penemuannya terkait atom, dimana ia menjelaskan bahwa pada atom terdapat gerakan partikel seperti electron yang mempunyai sifat gelombang. Oleh sebab itu, berlaku hukum-hukum gelombang pada teori atom modern yang ia kemukakan
Pada tahun 1926 Erwin schrodinger menegemukakan sebuah teori yang mana menurutnya electron sama dengan gelombang, selain itu ia juga menyatakan bahwa atom hanya bisa ditentukan daerah kemungkinan keberadaannya, daerah tersebut dinamakan orbital.
Orbital-orbital dengan tingkat energi yang sama atau nyaris sama akan membentuk subkulit, kumpulan beberapa sub kulit akan membentuk kulit
Dengan kata lain kulit terdiri dari beberapa sub kulit dan sub kulit terdiri dari beberapa orbital.
Modern atom dengan lintasan electron ini disebut sebagai model atom modern atau model atom mekanika kuantum yang berlaku hingga saat ini.
Pengertian Nomor Atom dan Nomor Massa
Suatu atom biasanya terdiri dari tiga pertikel utama yaitu proton yang bermuatan positif, electron yang bermuatan negarif, dan neutron yang tidak memiliki muatan sama sekali / netral.
Partikel-partikel ini sangat menentukan sifat dari suatu atom. Atom bersifat netral apabila jumlah proton dan electron harus seimbang. Jumlah muatan dalam suatu atom juga menentukan nomor massa dan nomor atom.
Nomor massa dan nomor atom adalah dua nomor yang terdapat dalam suatu atom yang menggambarkan jumlah pertikel yang ada pada suatu atom.
Tiap-tiap atom mempunyai jumlah proton, electron, dan neutron yang berbeda-beda.
Nomor atom atau nomor proton ( symbol “Z” ) adalah jumlah proton yang ditemukan di dalam inti atom. Karena atom bersifat elektronetral maka jumlah proton suatu atom sama dengan jumlah elektronnya.
Nomor massa atau nomor nucleon ( symbol “A” ) adalah jumlah total proton dan neutron dalam inti atom.
Cara Menentukan Nomor Atom dan Massa Atom
Cara mentukan nomor atom dan massa atom sangat mudah, kita hanya perlu memahami bentuk baku dari lambing suatu atom.
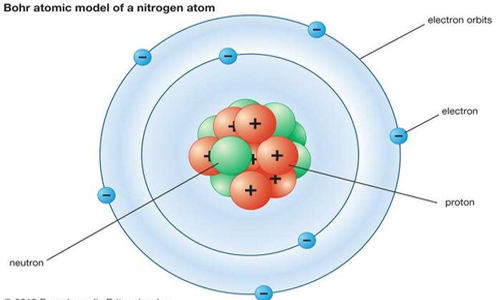
Perhatikan gambar berikut ini ;
Keterangan :
X = lambang unsur
A = nomor massa
Z = nomor atom
Agar lebih jelas perhatikan penjelasan di bawah ini ;
Dari gambar di atas kita peroleh N = lambang dari atom nitrogen, nomor massa nya 14, dan nomor atom nya 7.
Begitulah cara menentukan nomor massa dan nomor atom.
Demikian pembahasan kita kali ini tentang nomor atom dan massa atom, semoga artikel ini bisa bermanfaat dan menambah pengetahuan para pembaca sekalian.
Terima kasih.